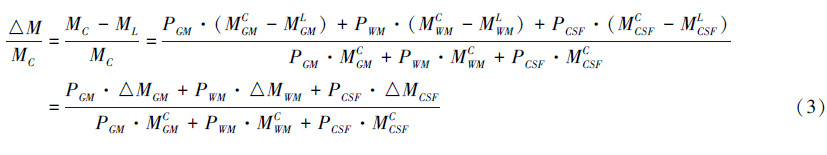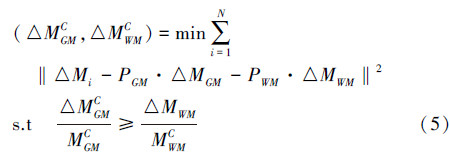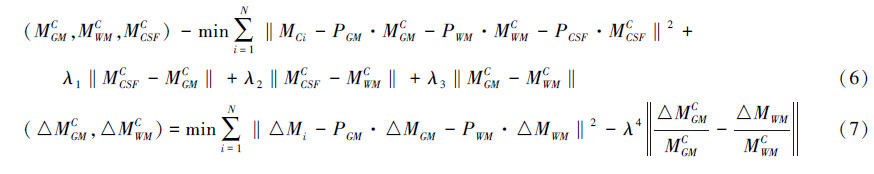2. 西安通信学院, 陕西 西安 710072
老年痴呆症,是一种常见于60岁以上老年人群中的持续性脑神经功能系统障碍疾病[1],在全世界被认为是继心脏病、癌症、中风之后导致人类死亡的“第四大杀手”[2]。据联合国《世界人口展望》报告统计:在2006年全球已确诊的失智症患者已达到2 660万人,到2050年全球每85人中预计就会有1人患有老年痴呆症[3]。根据卫生部2012年的统计数据:在我国现有的1.78亿60岁以上老年人中确诊的老年痴呆症患者就超过750万[4];加上其他由于自身并未意识到患病而未就医的 "隐形患者",我国老年痴呆症患者的数量可能已过千万。对于已进入人口老龄化社会的我国来说,老年痴呆症在现在以及未来的很长一段时间内都会是一个亟待解决的医疗和社会问题[4]。
尽早、准确地确诊患者病情,将有助于医生为患者制定治疗方案和开展后续治疗工作,达到最大程度缓解和抑制患者病情的目的。总体来说,诊断老年痴呆症的常用手段有3种,它们是:1)研究患者病史;2)对患者进行认知测试;3)对患者进行脑部成像扫描。研究患者病史是因为老年痴呆症患者的病情可能会由患者其他的常见并发症加深和复杂化(例如中风、心脏病、肾衰竭等),研究患者病史将有助于医生筛选患者多样病状中可以被治愈的部分。认知测试是对被测试者的记忆力、逻辑思维、执行等能力进行测试,从而判断被测试者是否患有老年痴呆症的手段。国际上流行的认知测试手段包括:简短精神状态测试(mini-mental state examination)[1]、亚当布鲁克认知测试(addenbrooke′s cognitive examination)[2]等。这类认知测试的好处在于:不需要对医生进行额外的复杂技术培训、测试操作简单易行。然而,这类测试的缺点也不容忽视:认知测试的结果通常受被测试者的教育背景和生活经历影响很大,容易导致医生误诊。一般来说,一位未经历教育的被测试者的逻辑思维能力一般比一位受过教育却患有轻度痴呆症的被测试者逊色,前者普通人的测试分数会低于后者患者。有鉴于此,对患者脑部进行成像扫描已经成为了如今在绝大多数医院和研究机构中诊断患者老年痴呆症病情的重要手段。
诊断痴呆症的脑部成像方式有多种,常用的包括有:计算机断层成像(computed tomography,简称CT)、正电子发射计算机断层扫描(positron emission tomography,简称PET)、单光子发射计算机断层扫描(single-photon emission computed tomography,简称SPECT)、磁共振成像(magnetic resonance lmaging,简称MRI)等。其中,MRI作为一种无放射性的成像方式,因其可以提供比其他成像方式更高的对比度和空间分辨率,而被广泛运用在大脑、心脏、乳腺等人体重要器官的成像中。结构性磁共振成像(structural MRI,简称sMRI)和功能性磁共振成像(functional MRI,简称fMRI)在痴呆症研究和诊断中获得了广泛运用[3, 4]。结构性磁共振成像能提供高分辨率的大脑结构和大脑组织细节影像,它有助于医生通过观察患者的大脑萎缩程度来确定患者痴呆症的病情(这是由于痴呆症的病理主要表现在患者大脑皮质的弥漫性萎缩、沟回增宽、脑室扩大和神经元大量减少等,造成患者的大脑构造与正常人有所不同)。在近几年来,基于结构性磁共振成像研究痴呆症的代表性工作包括研究大脑的整体结构变化、内嗅皮层、海马体、颞叶等组织结构的萎缩程度等[3],作为判断患者是否患有痴呆症及其严重程度的重要依据。功能性磁共振成像则通过测量患者大脑神经元活动所引发的一系列血液流动变化,来判断患者的大脑功能运转是否正常。由于痴呆症患者的大脑萎缩会造成其所需的血氧消耗比正常人要低,因此,能反映大脑血氧消耗的功能性磁共振成像作为一种研究老年痴呆症的重要手段,在近年来得到了广泛关注[4]。
在国内外现行的通过研究患者MRI影像来诊断患者痴呆症病情的工作中,模式识别、图像处理等领域的知识与技术被广泛运用在建立各类患者病情预测模型中[5, 6, 7]。在文献[5]中,ADNI标准数据库中每位患者的结构性磁共振成像中不同区域的脑皮层厚度被用来组成了反映不同患者脑皮层特性的形态学模式,并被运用在支持向量机中来预测患者是否患有轻度认知损害。在文献[6]中,研究者针对现行的大多数研究工作中通常会遇到的患者影像数据维度过高以及患者数量相对较少的典型模式识别维度诅咒问题,运用近年来在模式识别领域流行的稀疏表征思想来构造多重模式分类器,以此提高预测患者病情的确诊率。在文献[7]中,患者大脑被分割成为灰质、白质、脑脊髓液等3个组成部分;在每个部分中,特定区域的体积被用来作为反映患者病情的重要因素,并运用支持向量机来判断患者病情。
在本文中,动脉自旋标记(arterial spin labeling,简称ASL)这种新颖的功能性磁共振成像方式被运用在患者的老年痴呆症诊断中。相比较传统的MRI成像方式,ASL的最大好处是:它不需要对患者额外注射造影剂(例如钆等重金属),是一种完全无侵入、对患者完全安全的磁共振成像方式。ASL的其他优点也包括:可以作为与结构性磁共振成像同时实施的成像方式;具备扫描成本低、扫描时间短等优势。国际上第一批将ASL与老年痴呆症联系在一起的相关研究成果在2011~2012年被报道[8, 9]。在国内类似的研究工作还未系统开展。
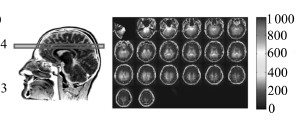
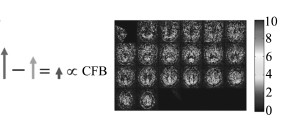
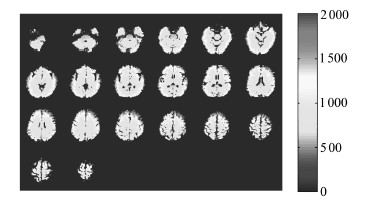
1 动脉自旋标记图像及部分容积效应问题与其他成像方式类似,ASL也需要借助一类“追踪器”来成像。与PET等使用具有放射性的正电子发射核素不同,ASL的“追踪器”是经过磁性标记过的动脉血液中的水分子,因此ASL无放射性、对人体完全安全。采集的ASL图像可由标记图像和标准图像两部分得到。采集标记图像包括以下步骤:首先,动脉血液进入一个事先设定好的观测区域(region-of-interest,简称ROI)之前,会经一个180°的无线电频率反转脉冲信号进行磁性激化标注(图 1左部1号区域代表该标注区域)。经过一个渡越时间后,这一部分带有磁性标记水分子的动脉血液会随人体血液循环作用进入ROI区域(图 1左部2号区域)。此时,带有磁性水分子的动脉血液会改变ROI区域内的磁化强度,进而影响磁共振扫描仪线圈的接收信号,产生标记图像。图 1右部为一位患者标记图像的横断面视角实例,单位为mL/(100g*min)。而对于标准图像来说,它的采集不需要经过类似的磁性标注(图 2左部的3号区域无磁性标注),而在相同的ROI区域内(图 2左部4号区域表示)直接获得标准图像。图 2右部中为同一位患者标准图像的横断面视角实例。对比可以看出:尽管标记图像和标准图像在视觉上很相似,这两部分图像在大脑的某些区域会存在差异;而这部分差异将正比于患者的大脑血流量(cerebral blood flow,简称CBF)。将标准图像和标记图像直接相减即可获得反应患者大脑血流量的ASL图像:图 3右部为同一位患者ASL图像的横断面视角实例。由于老年痴呆症患者较未患病的正常人在大脑的特定区域中会存在萎缩现象,这些区域的大脑血流量会相应变低。因此,能定量反映大脑血流量信息的ASL图像可以被作为诊断患者痴呆症病情的客观图像依据。
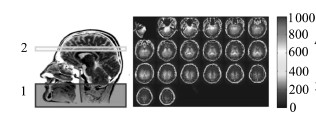 |
| 图 1 采集标记图像示意图及其实例 |
 |
| 图 2 采集标准图像示意图及其实例 |
 |
| 图 3 利用标记和标准图像差生成ASL图像及其实例 |
部分容积效应(partial volume effect,以下简称PVE)是ASL图像处理中不能规避的关键问题。一般来说,PVE的产生与由于ASL图像的像素异质性所导致的信号相叉污染有关。PVE现象特指:当被扫描物体(例如本文中的大脑组织区域)小于扫描硬件空间分辨率半峰全宽的2倍时,所造成的被扫描物体合成活性(resultant activity,例如本文中的大脑血流量)被低估的问题。一般来说,由于大脑灰质区域主要由神经元、神经胶质细胞和毛细血管组成,该区域的血流量会大于白质和脑脊髓液区域的血流量。但由于PVE现象的存在,ASL图像的灰质区域会受到白质和脑脊髓液等区域信号的交叉影响,使得灰质区域中实测的大脑血流量降低。因此,被PVE现象所影响的ASL图像的直接表征是:其灰质区域大脑血流量偏低。PVE问题的数学表述如下。对于ASL图像内每个像素点,它的标准磁化强度MC和标记磁化强度ML可以被表示为:
式中,PGM、PWM、PCSF代表该像素点上灰质、白质、脑脊髓液各部分所占的比例;这3个量可以通过FSL工具箱直接分割磁共振图像获得,故为已知量。由临床经验可以得到:ASL图像内脑脊髓液部分的标准磁化强度和标记磁化强度一般相同(MCSFC=MCSFL)。因此,对于ASL图像内的每个像素点,方程1和2总共包含5个未知数: 灰质区域标准磁化强度MGMC、白质区域标准磁化强度MWMC、脑脊髓液区域标准磁化强度MCSFC、灰质区域标记磁化强度MGML、白质区域标记磁化强度MWML。为了求解上述(2个方程5个未知数)的不定方程问题,现行普遍方法是将待求解像素点周围某个最近邻域内其他像素点的信息引入。以待求解像素点周围3×3共9个像素点的最小邻域为例:这些像素点上的已知量PGM/PWM/PCSF可以作为矩阵元素构造出一个9×3大小的回归核矩阵P(其中矩阵列数由PGM、PWM、PCSF产生);此外,待求解像素点本身的标准磁化强度和标记磁化强度都为已知的观测量(记为矩阵M);由上述信息即可通过线性回归最小二乘法(PTP)-1PTM来求解方程中的未知数,其中T表示矩阵的转置[14]。这类方法虽然容易理解并且操作简单,但由于需要额外引入目标像素最近邻域内其他像素信息进行方程组求解,容易造成处理后的图像过平滑及大脑组织内细节信息严重丢失等突出问题。图 4是运用上述方法在已采集的一位患者ASL图像实例中求解灰质区域标准磁化强度MGMC的结果。由于绝大多数在目标像素最近邻域内的像素点在求解目标像素的周围像素过程中都会被重复使用,求解结果的过平滑和大脑组织内细节信息丢失等问题就变得显而易见。这样得到的图像结果会给后续基于ASL图像的患者痴呆症病情诊断带来极大的负面影响。
 |
| 图 4 采用线性回归算法求得某位患者的MGMC |
要从根本上避免上述过平滑和细节丢失问题,需要在改善部分容积效应时只运用单个像素点自身的信息,而不引入其最近邻域内的其他像素点信息。为了实现基于单像素点信息的PVE改善,在采集患者ASL图像的磁共振扫描过程中,可以通过对患者进行重复扫描来提高ASL图像的信噪比和获取关于单像素点的额外信息。以下为说明方便,首先将归一化ASL磁化改变强度△M/MC描述如下:
式中,△MGM和△MWM分别为灰质区域和白质区域的ASL磁化改变强度;△MCSF是脑脊髓液区域ASL磁化改变强度(但由于MCSFC=MCSFL,使得△MCSF=0)。与PVE问题的原始方程组类似,方程(3)中部分容积改善的5个待求解未知数为:△MGM、△MWM、MGMC、MWMC、MCSFC。假定采集ASL图像序列的重复扫描次数为N,方程(3)的未知数求解可以转化为下列最优化问题: 式中,i代表第i次扫描。上述方程的约束条件表示大脑不同区域的磁化强度关系(即脑脊髓液区域的磁化强度不小于灰质区域和白质区域的磁化强度、灰质区域的磁化强度不小于白质区域的磁化强度;大脑灰质区域的ASL信号要强于白质区域的ASL信号等)。方程(4)和(5)可以通过拉格朗日乘数法改写为如下形式: 式中,λ为拉格朗日乘数。上述方程是本文提出的基于ASL图像单个像素点信息改善部分容积效应新算法的一般数学表达式。为了求解方程(6)和(7)中的未知数,本文采用一种基于Split-Bregman思想的求解方法[15]。对于方程(6),利用Split-Bregman思想求解未知数MGMC、MWMC和MCSFC的算法步骤如下所述:对于每个像素点,输入的已知量是在该像素点上大脑分割出的灰质、白质、脑脊髓液等区域所占的比例:PGM、PWM、PCSF,以及在该像素点上第i次扫描所测量的标准磁化强度MC,i。Split-Bregman思想主要基于迭代步骤:在第k次迭代中按照所示的3个步骤求解方程(6)的3个未知量:首先是在获得的上一步(第k-1次迭代)该像素点白质区域和脑脊髓液区域标准磁化强度MWMC,k-1、MCSFC,k-1的基础上构造一个二次规划问题,并求解第k次迭代中的MGMC,k。这类二次规划问题的求解方法有很多,本文采用内点法求解。然后再分别求解MWMC,k和MCSFC,k,思想与第一步类似。当相邻2次未知量迭代求解差值的最大范数小于或等于一个事先设定好的足够小的容忍阈值时停止,此时的求解结果即为该像素点上MGMC、MWMC和MCSFC的结果。 求解方程(7)中的2个未知量△MGM和△MWM也采用类似的方法。由上述步骤描述可知,本文提出的基于ASL图像单个像素点信息进行部分容积效应改善的新思想中并没有像现行改善方法一样借助像素点周围的最近邻域内其他像素信息,而是运用待改善的目标像素点自身的信息、通过多次扫描获得该像素点额外信息以及大脑区域磁化强度之间的约束关系来构造最优化问题,求解方程(6)和(7)以达到改善目标像素点部分容积效应的目标。图 5是在与图 4相同的患者的ASL图像数据上采用上述新算法的改善结果。可以看出:新算法(图 5结果)能有效抑制现行方法(图 4结果)中存在的过平滑和大脑组织细节信息丢失等严重问题。
 |
| 图 5 采用本文新提出算法在图4同一位患者数据上求得的MGMC |
为了展示新算法较现有部分容积效应改善算法的优势,一个由360名患者数据所组成的数据库被运用在本文的实验部分。这些患者的数据由南昌大学附属医院采集。这360名患者可以按照老年痴呆症的病症严重程度分为3类:阿尔茨海默病(alzheimer′s disease,简称AD)、轻度认知损害(mild cognitive impairment,简称MCI)、无认知损害(non cognitive impairment,简称NCI),每一类病症的患者数量都为120名。该数据库内患者的平均年龄是70.56±7.20岁。所有磁共振图像均有西门子3T TIM Trio磁共振扫描仪采集;每位患者获取ASL图像的重复扫描次数是23次。其他采集的参数包括:标记持续时间1 500 ms、后标记延迟1 500 ms、ASL图像像素大小3 mm×3 mm×5 mm。高分辨率的结构磁共振图像(磁化准备快速梯度回波图像)也会在扫描每一位患者时同时获得。完成图像采集以后,运动修正会在磁共振图像中实施;图像在完成大脑组织提取后,会进一步被分割成灰质、白质、脑脊髓液三部分。所有上述分割结果均会在ASL图像和结构磁共振图像间完成相互配准。以上所有步骤均通过SPM8软件完成。
3.2 ASL图像容积效应改善实验分析根据之前所述,ASL图像中的部分容积效应会造成大脑血流量CBF被低估;因此,越有效的部分容积效应改善算法就能更大程度的提高ASL图像中的CBF数值。本文中提出的基于单像素点信息的新型改善算法(简写为“New”)与现行的基于最近邻域像素点的改善方法(简写为“RB”)进行了比较。在RB方法中,不同的最近邻域范围被复现以观察不同大小情况下的最近领域对部分容积效应改善效果的好坏,3种不同的最近领域范围5×5,9×9,15×15被用来说明最近领域偏小、中等、偏大3种情况(对应改善方法分别记为“RB-5”、“RB-9”和“RB-15”)。图 6~图 8的统计箱图揭示了对于不同痴呆症程度(图 6对应AD患者情况、图 7对应MCI、图 8对应NCI)。
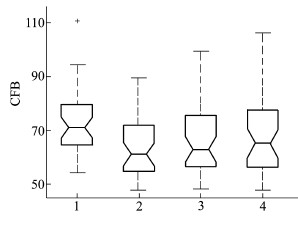 |
| 图 6 AD患者改善大脑血流量的统计箱图 |
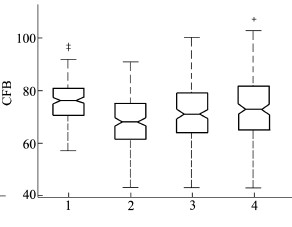 |
| 图 7 MCI患者改善大脑血流量的统计箱图 |
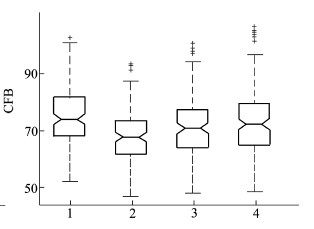 |
| 图 8 NCI患者改善大脑血流量的统计箱图 |
在图 6~图 8的每个统计箱图中,水平中线代表了不同方法所计算出的患者CBF中位数;统计箱的上下边缘由2条水平直线表示,它们代表了所计算出的患者CBF上四分位数和下四分位数;每个统计箱的四分位数外都有一条垂直的虚线,虚线的范围是1.5倍的四分位数间距;超过1.5倍四分位数间距的患者实例由离散的加号所表示。由图 6~图 8可以观察到:本文所介绍的新算法所产生的CBF明显高于其他比较方法的产生结果,这表明被部分容积效应所影响而被低估的CBF数值被本文介绍的新算法改善效果最突出。
上述实验的定量化统计分析如下。表 1~表 3分别描述了对于AD、MCI、NCI病状的多项比较实验的结果。表中的结果提供了2类分析手段:一类是单值估计,它描述了方法1与方法2计算的CBF差异(方法1-方法2);另一类是区间估计,它描述了方法1与方法2计算的CBF差异有可能落入的区间(95%的置信概率)。从表 1~表 3的结果可以看出,主要的计算结果都为正值。这说明方法1(即本文介绍的新方法“New”)获得改善后的CBF值较方法2(即各类基于最近领域的现行比较方法“RB”)获得改善后的CBF值普遍更高,部分容积效应改善效果更好。尽管表 2~表 3中个别区间统计下确界出现了负值情况,但表 4将所有AD、MCI、NCI的统计结果在一起考虑后可以看出:本文提出的新方法在基于360个患者的数据库中的总体改善结果要优于其他比较的现行方法。这在统计上说明了本文介绍的新方法改善容积效应的优越性。
| 方法1 | 方法2 | 单值估计 | 区间估计 |
| New | RB-5 | 10.140 6 | [3.407 0,16.874 2] |
| New | RB-9 | 7.440 9 | [0.707 2,14.174 5] |
| New | RB-15 | 5.593 8 | [-1.139 8,12.327 4] |
| 方法1 | 方法2 | 单值估计 | 区间估计 |
| New | RB-5 | 7.795 5 | [4.941 9,10.649 1] |
| New | RB-9 | 4.687 3 | [1.833 7,7.540 9] |
| New | RB-15 | 2.854 9 | [0.001 3,5.708 5] |
| 方法1 | 方法2 | 单值估计 | 区间估计 |
| New | RB-5 | 6.270 9 | [2.853 6, 9.688 2] |
| New | RB-9 | 3.096 1 | [-0.321 3, 6.513 4] |
| New | RB-15 | 1.315 7 | [-2.101 6, 4.733 1] |
| 方法1 | 方法2 | 单值估计 | 区间估计 |
| New | RB-5 | 7.479 7 | [5.376 6,9.582 7] |
| New | RB-9 | 4.390 4 | [2.287 3,6.493 5] |
| New | RB-15 | 2.575 8 | [0.472 7,4.678 9] |
在这一部分中,传统的有监督和无监督模式识别工具被运用在改善后的ASL图像中,来进行患者痴呆症病情严重程度的预测诊断。每位患者的改善后ASL图像中与判断痴呆症密切相关的大脑区域组织,包括海马体、尾壳核、海马旁回、丘脑等4个区域,都被SPM扩展软件分割出来。在这些分割区域中,MCMC和MCML的均值被计算出来组成一个8维的向量特征来表征每一位患者的信息。4种经典的模式识别工具,包括线性回归(linear regression,简称LR)、k-means聚类(简称k-means)、支持向量机(support vector machine,简称SVM)、排序支持向量机(ranking-SVM,简称rSVM)等方法被复现,来实现基于改善后ASL图像的患者病情严重程度预测判断。本实验采用的由360名患者组成的数据库被平均分割成6个子集,以进行一个6重交叉验证实验。对于有监督工具(包括LR、SVM、rSVM)来说,每重实验中有5个子集被用来实现这些监督工具中未知参数的学习(包括LR中的回归系数、SVM和rSVM中采用的高斯半径基核函数的高斯宽度等),剩下的1个子集作为每重实验的测试集。对于无监督工具(包括k-means)来说,没有训练阶段,测试直接进行。基于不同部分统计效益改善算法产生的ASL图像进行病情程度预测的统计结果如表 5所示。可以看出,本文新提出的改善算法所产生的ASL图像在所复现的3个模式识别工具中(包括LR、SVM、rSVM)较现行改善算法所产生的ASL图像能取得更准确的病情预测判断结果(即预测结果与医生判断结果之间的误差最小)。由于本文新提出的改善算法能避免过平滑和大脑细节信息丢失等严重问题,因为改善后的ASL图像能保留尽可能多的大脑组织信息细节,这对于具备判断性的模式识别工具(例如SVM、rSVM等)更有帮助。所以能在相应的工具中取得更优的实验结果。从表 5还可以看出,本文新提出的改善算法与rSVM组合可以在所采用的包含360名患者的数据库中获得最高的预测准确度。
| 方法 | LR | k-means | SVM | rSVM |
| New | 0.597 1±0.031 9 | 0.539 7±0.003 8 | 0.817 1±0.051 7 | 0.917 1±0.032 0 |
| RB-5 | 0.585 7±0.034 3 | 0.544 1±0.013 8 | 0.757 1±0.064 7 | 0.795 6±0.015 5 |
| RB-9 | 0.568 6±0.036 9 | 0.537 1±0.003 2 | 0.737 9±0.026 9 | 0.787 9±0.023 3 |
| RB-15 | 0.594 3±0.036 9 | 0.543 8±0.023 2 | 0.757 6±0.011 3 | 0.765 9±0.012 3 |
在本文中,一种基于单像素点信息的新颖的ASL图像部分容积效应改善算法首次被提出。这种新算法区别于现行部分容积效应改善算法的优势在于:(1)在获取ASL图像的采集阶段创新性的加入了对患者重复扫描以在同一扫描区域获得多张ASL图像的扫描策略,这些信息不仅增强了原始ASL图像的信噪比,同时为基于单像素点改善容积效应提供了更多像素点自身的信息;(2)将部分容积效应改善的问题看做是一个有约束的最优化问题,并创新的引入了Split-Bregman思想进行求解。本文的科研贡献在于:不仅提出该新算法本身,还展示了新算法比较现行改善算法在老年痴呆病症严重程度的预测诊断这一重要运用中的良好的运用前景。本文之后的研究工作将集中在提出更多的病情预测模型来构造整体预测系统,最大程度上提高基于ASL图像的患者痴呆症病情预测准确度。
| [1] | Mahendra B. A Pathography of Dementia[J]. Dementia, 1987(1): 189-202 |
| Click to display the text | |
| [2] | Folstein M, Folstein S, McHung P. Mini-Mental State: A Practical Method for Grading the Cognitive State of Patients for the Clinician[J]. Journal of Psychiatric Research, 1975, 12(3): 189-198 |
| Click to display the text | |
| [3] | Cardenas V, Chao L, Studholme C, et al. Brain Atrophy Associated with Baseline and Longitudinal Measures of Cognition[J]. Neurobiology of Aging, 2011, 32(4): 572-580 |
| Click to display the text | |
| [4] | Wee C, Yap P, Denny K, et al. Resting-State Multi-Spectrum Functional Connectivity Networks for Identification of MCI Patients[J]. PLoS Computational Biology, 2012, 7(5): e37828 |
| Click to display the text | |
| [5] | Wee C, Yap P, Shen D. Prediction of Alzheimer's Disease and Mild Cognitive Impairment using Cortical Morphological Patterns[J]. Human Brain Mapping, 2013, 34(12): 3411-3425 |
| Click to display the text | |
| [6] | Liu M, Zhang D, Shen D. Ensemble Sparse Classification of Alzheimer's Disease[J]. Neuro Image, 2012, 60(2): 1106-1116 |
| Click to display the text | |
| [7] | Zhou L, Wang Y, Li Y, et al. Hierarchical Anatomical Brain Networks for MCI Prediction: Revisiting Volumetric Measures[J]. PLoS Computational Biology, 2011, 6(7): e21935 |
| Click to display the text | |
| [8] | Malpass K. Alzheimer Disease: Arterial Spin-Labeled MRI for Diagnosis and Monitoring of AD[J]. Nature Reviews Neurology, 2012, 8(1):3 |
| Click to display the text | |
| [9] | Chen Y, Wolk D, Reddin J, et al. Voxel-Level Comparison of Arterial Spin-Labeling Perfusion MRI and FDG-PET in Alzheimer Disease[J]. Neurology, 2011, 77(2): 1977-1985 |
| Click to display the text | |
| [10] | Asllani I, Borogovac A, Brown T. Regression Algorithm Correcting for Partial Volume Effects in Arterial Spin Labeling MRI[J]. Magnetic Resonance in Medicine, 2008, 60: 1362-1371 |
| Click to display the text | |
| [11] | Goldstein T, Osher S. The Split Bregman Method for L1 Regularized Problems[J]. UCLA CAM Report, 2008, 8(29): 1-21 |
| Click to display the text |
2. Xi'an Communication Institute, Xi'an, 710072, China