离子液体是由纯离子组成,室温下呈液态的物质,具有液程宽、蒸汽压低、溶解能力强、电导率高等特点,广泛应用于电化学、分离、催化等诸多领域。虽然磁性离子液体的潜在应用价值很大,但其研究起步较晚,2004年由 Hayashi 等[1]首次报道了磁性离子液体[C4mim]FeCl4,近年来该方面的研究也受到越来越多学者的关注,Soheil等[2]制备了[C2OHmim]FeCl3Br-并作为合成1-氨烷基-2-萘酚的催化剂,表现出较强的催化活性,且产率较高;Raquel等[3]利用正常皮肤纤维细胞和大肠癌、腺癌细胞2种细胞模型在体外研究了不同磁离子液体阴阳离子的毒性。此外,离子液体作为一种新型环保介质,不易挥发,化学性质稳定,在环境保护领域发挥着重要作用。离子液体的阴离子具有较强的氢键碱性[4],并可进一步引入胺基等功能化基团提高碱性[5],因此具有选择性分离CO2和SO2的潜力。Kuan[6]等合成3种新的二羧酸盐酸羟胺离子液体对SO2进行吸收,其吸收能力为每摩尔离子液体吸收SO20.1~0.6 mol。
本文合成了1-甲基-3-丁基咪唑四卤化铁([C4mim]FeCl4和[C4mim]FeBrCl3)2种磁性离子液体,对其结构、密度及磁性能进行了表征,研究了这2种磁性离子液体的吸收特性,为今后磁性离子液体的应用研究提供了参考。
1 实验方法 1.1 试剂N-甲基咪唑(阿拉丁试剂有限公司)分析纯;溴代正丁烷、氯代正丁烷(上海山浦化工有限公司)分析纯;无水三氯化铁(阿拉丁试剂有限公司)分析纯;乙酸乙酯、丙酮、乙醚、乙醇(天津星月化工有限公司)分析纯。
1.2 [C4mim]FeCl4与[C4mim]FeBrCl3的制备制备[C4mim]FeCl4反应式如下:
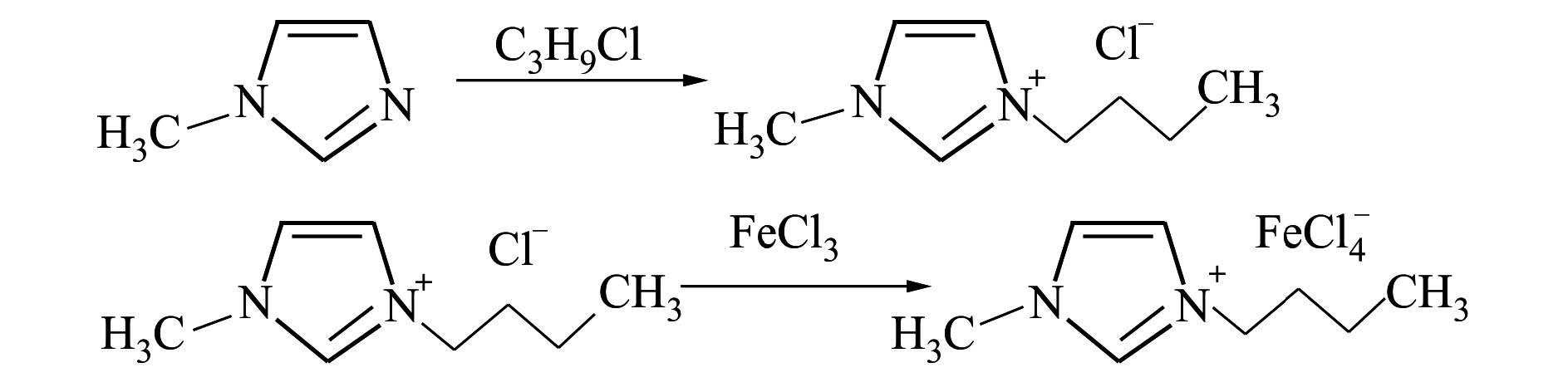
将一定量N-甲基咪唑置于250 ml 的装有回流装置的三口烧瓶中,快速搅拌,油浴加热,40 min内滴加等摩尔氯代正丁烷。温度调至70℃反应约24 h ,溶液变得较粘稠,最终变为金黄色液体。反应结束后静置冷却,加入适量的乙酸乙酯萃取分离3~4次,将未反应的原料完全除去。最终将产物加热至80℃,旋转蒸发除去乙酸乙酯,于100℃ 真空干燥48 h,得到1-甲基-3-丁基咪唑氯离子液体,即[C4mim]Cl。
将[C4mim]Cl和等摩尔量的无水三氯化铁在N2的保护下缓慢加入三口烧瓶中,络合反应约24 h,得深棕黄色液体。加去离子水萃取分离3次,将未反应的反应物彻底除去。将得到的棕黄色澄清液体于80℃下真空干燥48 h,得到1-甲基-3-丁基咪唑四氯化铁磁性离子液体,即[C4mim]FeCl4。[C4mim]FeBrCl3以N-甲基咪唑、溴代正丁烷与无水氯化铁为原料,制备方法同上。
1.3 表征用Thermo Scientific公司NIcolET iS10型红外光谱仪对磁性离子液体进行表征。由于磁性离子液体的磁性会对核磁共振仪测量信号产生干扰,所以只对磁性离子液体的中间产物[C4mim]Cl和[C4mim]Br进行1H-NMR 表征,仪器型号为Bruker400,以确定阳离子结构。采用Raman1000光谱仪对阴离子进行表征,以确定其结构。以鲁道夫公司生产的DDM2911数字式密度计测定磁性离子液体的密度,以Lakeshore公司VSM-7307振动样品磁强计分析产物的磁性能。
2 结果与讨论 2.1 FT-IR分析通过红外光谱对[C4mim]Cl与[C4mim]FeCl4、[C4mim]Br与[C4mim]FeBrCl3的结构进行表征。红外分析图谱见图1a)与图1b)。
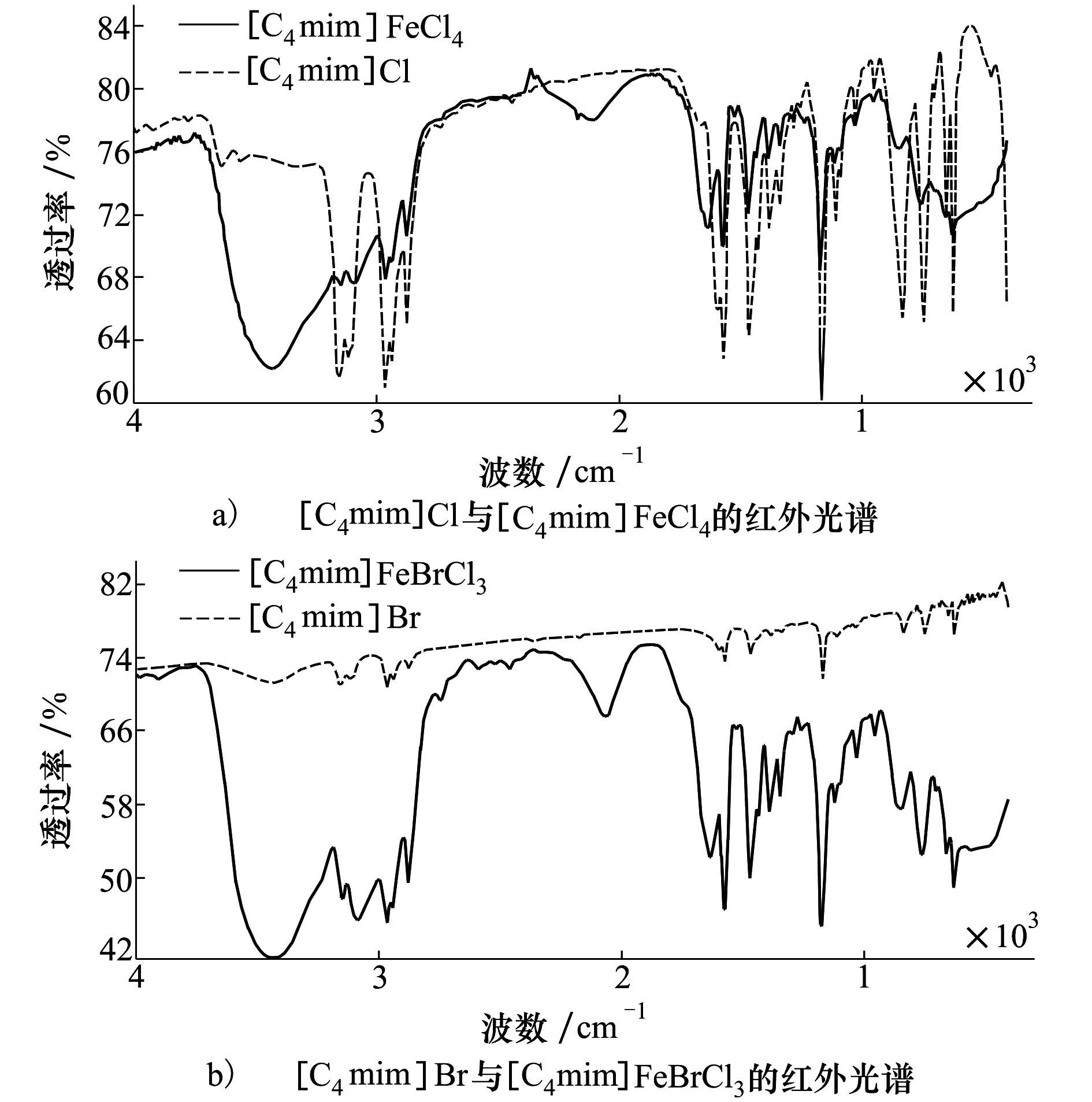 |
| 图 1 [C4mim]Cl和[C4mim]FeCl4与[C4mim]Br与[C4mim]FeBrCl3的红外图谱 |
对比中间体与它们相应的最终产物的红外光谱,可知所合成的2种磁性离子液体的阳离子和相应中间体中的阳离子结构一致。除了最终的磁性离子液体有更尖锐的峰之外,从指纹区(400~1 300 cm-1)到特征频率区(1 300~4 000 cm-1),两者无明显差异。因此,可推测阳离子[C4mim]+并没有参与配位,只是阴离子Cl-或Br-和FeCl3进行了络合反应,配合物的阴离子结构对配合物的化学位移影响很小。
2.2 [C4mim]Cl,[C4mim]Br的核磁共振分析通过核磁共振分析对[C4mim]Cl,[C4mim]Br 2种离子液体进行结构表征。其核磁共振分析数据见表1,谱图见图2。
| IL | 表征结果 |
| [C4mim]Cl | 0.89(t,3H),1.26(m,2H),1.80(m,2H), 3.72(m,3H),3.96(s,3H), 4.29(t,2H),7.94(s,1H),8.02(s,1H),9.74(s,1H) |
| [C4mim]Br | 0.95(t,3H), 1.37(m,2H), 1.91(m,2H), 4.13(s,3H),4.35(t,2H)7.64(s,1H), 7.76(s,1H),10.25(s,1H) |
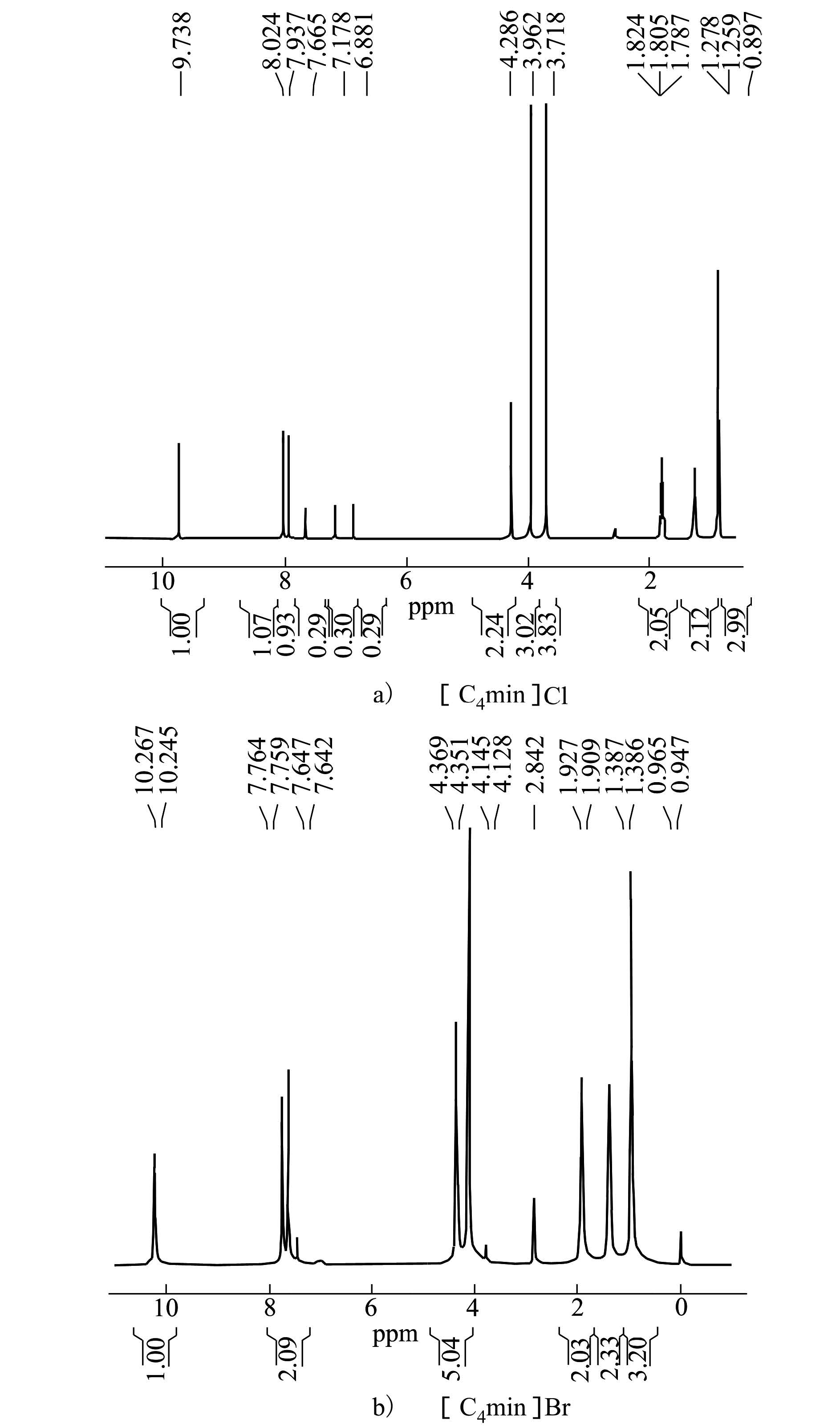 |
| 图 2 [C4mim]Cl与[C4mim]Br的核磁共振氢谱 |
由谱图与数据知,在一定误差范围内,峰面积的近似比与相应的氢原子个数比一致。谱图中没有多余峰出现,合成的离子液体和目标产物一致,因此成功制备了[C4mim]Cl,[C4mim]Br离子液体。
2.3 [C4mim]FeCl4,[C4mim]FeBrCl3的Raman光谱分析Raman光谱是表征离子液体阴离子结构的有效手段。利用Raman对[C4mim]FeCl4、[C4mim]FeBrCl3进行了结构表征,详见图3。
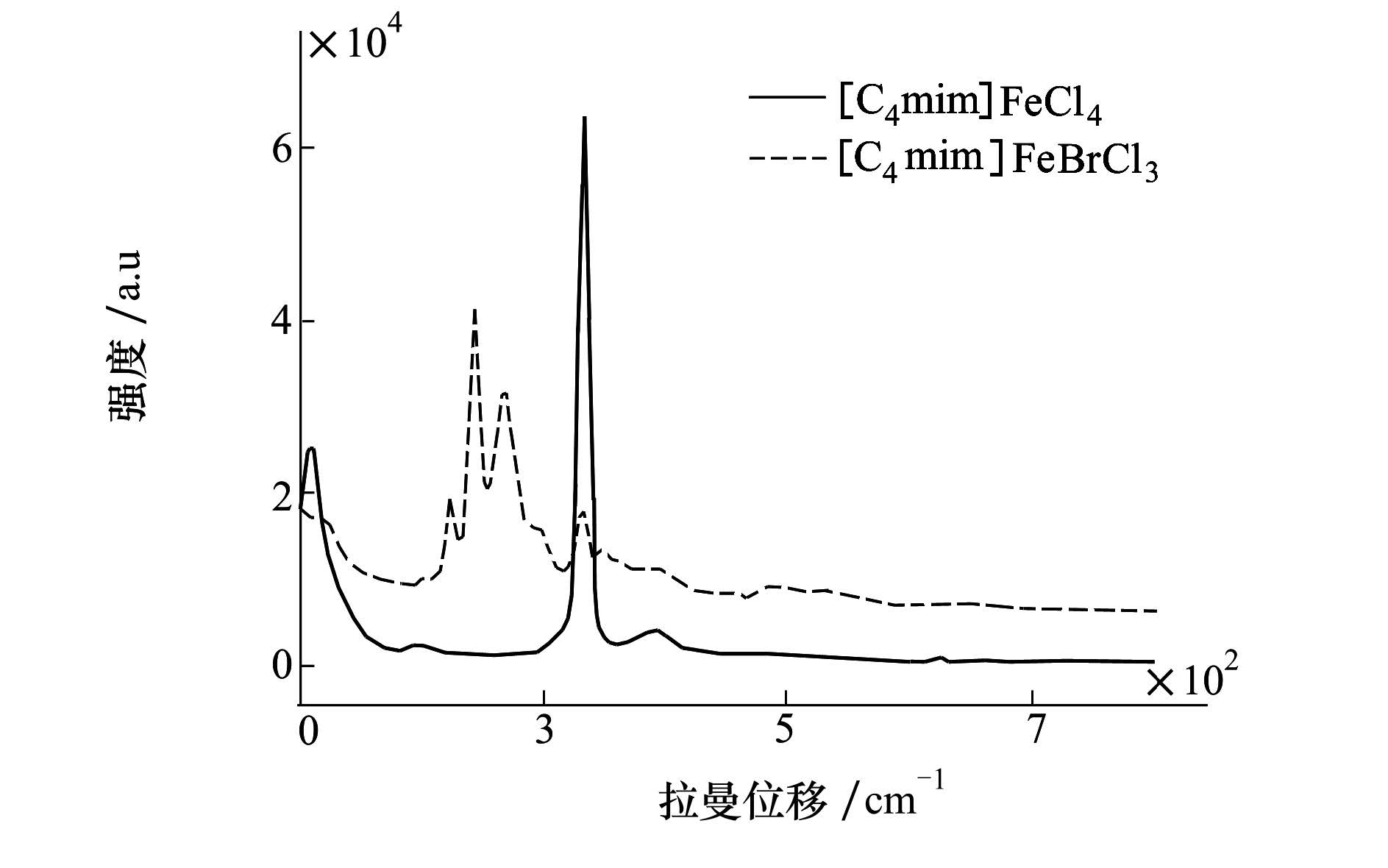 |
| 图 3 [C4mim]FeCl4和[C4mim]FeBrCl3的拉曼谱图 |
由图3可知,[C4mim]FeCl4共有2个特征峰:120 cm-1和330 cm-1。120cm-1处属于[C4mim]+阳离子特征峰,而330 cm-1处出现的较为尖锐的强峰,属于[FeCl]-阴离子特征峰。因此,所合成的离子液体阴离子均为[FeCl4]-,与目标产物一致。
而[C4mim]Br和FeCl3按照摩尔比1∶1进行反应时,除[FeBrCl3]-阴离子生成外,还含有不同配体结构阴离子生成。其反应机理可能为:当[C4mim]Br和FeCl3混合后,所生成的[C4mim]FeBrCl3为液体,未反应的 FeCl3和[C4mim]Br会很快溶于[C4mim]FeBrCl3液体中,并以Br-离子、Fe3+离子和Cl-离子形式存在,此时,这3种离子会自由的结合,生成例如[FeBr3Cl]-、[FeBr2Cl2]-、[FeCl4]-、[Fe2Br2Cl5]-等离子,而不是所谓完全纯的[FeBrCl3]-离子。
2.4 密度密度是磁性离子液体的一个易调变的重要物理性质。采用数字式密度计对[C4mim]FeCl4、[C4mim]FeBrCl3 2种磁性离子液体在20~80℃不同温度下的密度进行了测定,结果如图4所示。
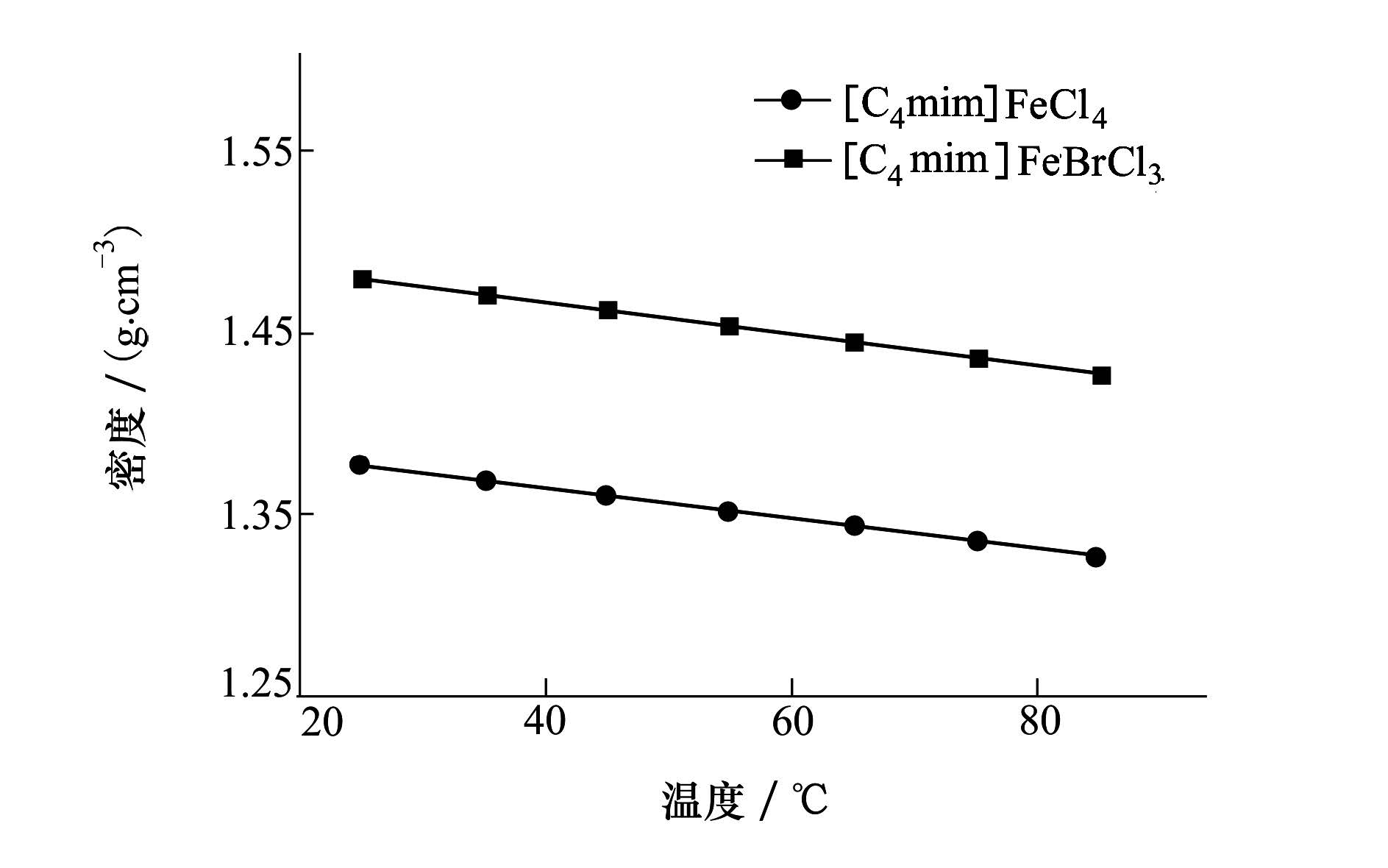 |
| 图 4 [C4mim]FeCl4,[C4mim]FeBrCl3的密度值随温度变化曲线 |
由图4可知,这2种磁性离子液体的密度/(g·cm-3)均随温度的升高而降低,但下降值较小,在温度由20℃增加至80℃过程中,密度减小量均在3.56%左右,故磁性离子液体的密度受温度的影响较小。[C4mim]FeBrCl3的密度比[C4mim]FeCl4大,这是因为阴离子体积稍有增加,相对质量大幅增加,故密度增大。
2.5 磁性能以振动样品磁强计对2种磁性离子液体[C4mim]FeCl4和[C4mim]FeBrCl3的磁性能进行分析,其磁化率随外加磁场强度变化关系见图5。
 |
| 图 5 磁性离子液体的磁化率与外加磁场强度的关系 |
由图5知,2种磁性离子液体的磁化率均随外加磁场强度的增强几乎呈线性增加,可知2种磁性离子液体在室温下为顺磁性物质。磁场强度为0Oe时,磁化率均为0emu/g左右。另外,相同温度、相同外加磁场强度条件下,[C4mim]FeCl4的磁化率要高于[C4mim]FeBrCl3的磁化率。这可能是由于[C4mim]FeBrCl3中的阴离子[FeBrCl3]-的不规则空间构型导致了其对应的磁性离子液体空间结构的无序化,而FeCl4相对于FeBrCl3具有更有序的空间排列,从而更易在外加磁场时形成有序排列。
2.6 对VOCs(挥发性有机物)的吸收环境中有机挥发物(VOCs)已成为环境中的重要污染物,对VOCs的吸收特性也成为磁性离子液体重要的应用之一。本文采用将挥发性有机气体(丙酮或乙醇)直接通入离子液体中的方法研究2种磁性离子液体[C4mim]FeCl4,[C4mim]FeBrCl3对其吸收特性。图6a)和图6b)分别为1g[C4mim]FeCl4或 [C4mim]FeBrCl3吸收丙酮、乙醇的质量与时间的关系曲线。
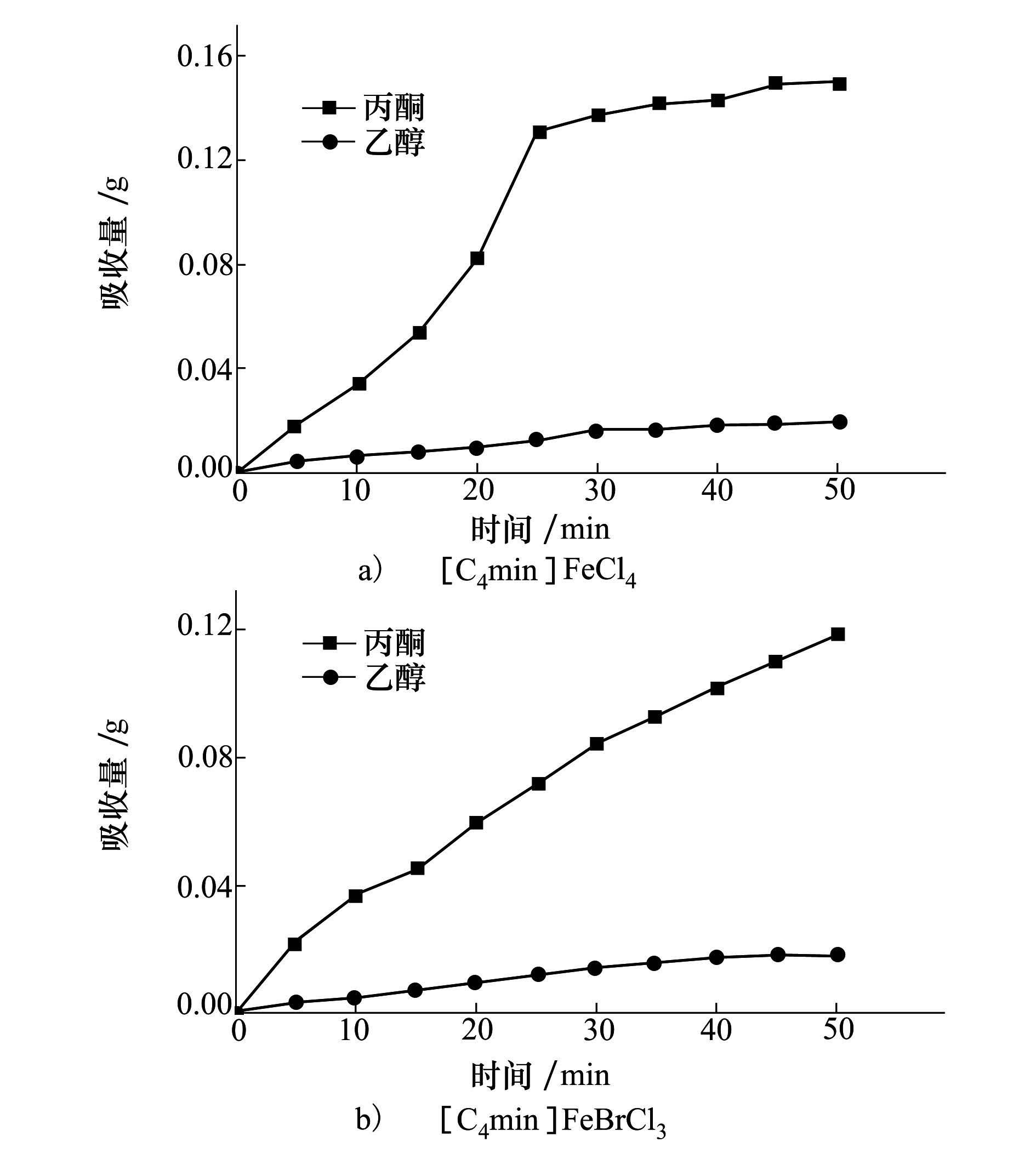 |
| 图 6 [C4mim]FeCl4与[C4mim]FeBrCl3 分别对丙酮及乙醇废气的吸收对比 |
图6中2种磁性离子液体对丙酮废气和乙醇废气都有一定的吸收。由图中可看出,在50 min内,1 g的[C4mim]FeCl4对丙酮废气和乙醇废气的吸收量分别约为0.150 g和0.018 g;1 g的[C4mim]FeBrCl3对丙酮废气和乙醇废气的吸收量分别约为0.172 g和0.019 g,得出2种磁性离子液体对丙酮有显著吸收,而对乙醇废气吸收效果不显著。
3 结 论1) 制备的磁性离子液体中,阳离子[C4mim]+并没有参与配位,只是阴离子Cl-或Br-和FeCl3进行了络合反应。
2) [C4mim]Br和FeCl3按照摩尔比1∶1进行反应时,除了生成[FeBrCl3]-阴离子外,还含有不同配体结构的阴离子生成。例如 [FeBr3Cl]-、[FeBr2Cl2]-、[FeCl4]-、[Fe2Br2Cl5]-等离子,而不是所谓完全纯的[FeBrCl3]-离子。
3) [C4mim]FeBrCl3的密度比[C4mim]FeCl4的大,二者的密度均随温度的升高而呈线性下降的趋势。
4) 2种磁性离子液体在室温条件下为顺磁性物质。相同温度、相同外加磁场强度条件下测得的[C4mim]FeCl4的磁化率要高于[C4mim]FeBrCl3的磁化率。
5) 2种磁性离子液体对丙酮有显著吸收,而对乙醇废气吸收效果不显著。
| [1] | Hayashi S, Hamaguchi H. Discovery of a Magnetic Ionic Liquid [bmim]FeCl4[J]. Chem Lett, 2004, 33(12): 1590-1591 |
| Click to display the text | |
| [2] | Soheil Sayyahi, Atena Azin, Seyyed Jafar Saghanezhad. Synthesis and Characterization of a Novel Paramagnetic Functionalized Ionic Liquid as a Highly Efficient Catalyst in One-Pot Synthesis of 1-amidoalkyl-2-naphtols[J]. Journal of Molecular Liquids, 2014, 198:30-36 |
| Click to display the text | |
| [3] | Raquel F M F, Simeonov S, Rosatella A A. Toxicological Evaluation of Magnetic Ionic Liquids in Human Cell lines[J]. Chemosphere , 2013, 92(1):100-105 |
| Click to display the text | |
| [4] | Poole C F, Chromatographic and Spectroscopic Methods for the Determination of Solvent Properties of Roomtemperature Ionic Liquids[J]. Journal of Chromatography A, 2004, 1037(1/2):49-82 |
| Click to display the text | |
| [5] | 赵旭, 邢华斌, 李如龙,等. 离子液体在气体分离中的应用[J]. 化学进展, 2011, 23(11):2258-2268Zhao Xu, Xing Huabin, Li Rulong, et al. Application of Ionic Liquids in Gas Separation[J]. Chemical Progress, 2011, 23(11): 2258- 2268 (in Chinese) |
| Cited By in Cnki (12) | Click to display the text | |
| [6] | Huang K, Lu J F, Wu Y T, et al. Absorption of SO2 in Aqueous Solutions of Mixed Hydroxylammonium Dicarboxylate Ionic Liquids[J]. Chemical Engineering Journal, 2013, 215(15):36-44 |

